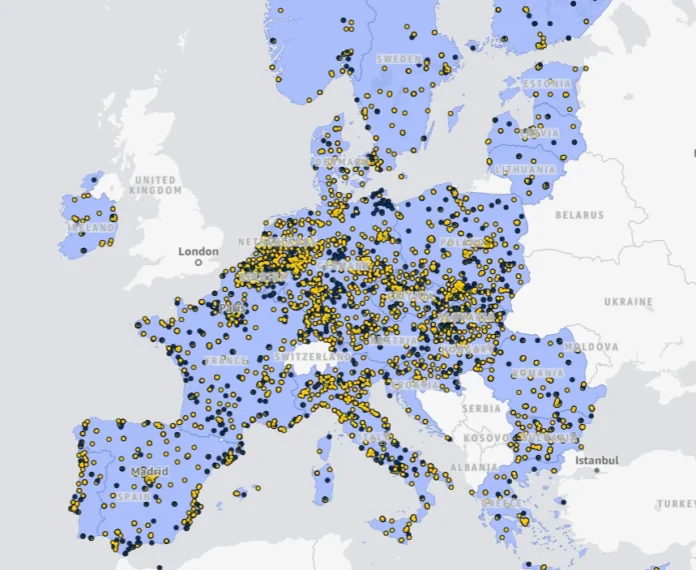
System Informacji o Badaniach Klinicznych (CTIS) wprowadził nową funkcję – interaktywną mapę badań klinicznych, która ma uprościć dostęp do informacji o trwających badaniach na terenie Unii Europejskiej. Inicjatywa ma na celu zwiększenie świadomości pacjentów i personelu medycznego na temat dostępnych badań oraz ułatwienie procesu rekrutacji uczestników.
Nowa funkcjonalność pozwala na wyszukiwanie badań według lokalizacji i jednostki chorobowej. Dodatkowo umożliwia kontakt z ośrodkami prowadzącymi badania, co może prowadzić do większego udziału pacjentów w eksperymentalnych terapiach.
Jak działa nowa mapa badań klinicznych?
Interaktywna mapa w systemie CTIS bazuje na publicznie dostępnych danych i oferuje kilka kluczowych funkcji:
- Wyszukiwanie badań według lokalizacji geograficznej – użytkownicy mogą sprawdzić, które badania są prowadzone w ich kraju lub regionie.
- Filtrowanie wyników według schorzenia – pacjenci i lekarze mogą łatwo znaleźć badania dotyczące konkretnych chorób.
- Zaawansowana wyszukiwarka z autokorektą – system podpowiada użytkownikom poprawne wyniki w przypadku literówek lub niepełnych zapytań.
- Dostęp do danych kontaktowych badaczy – zainteresowane osoby mogą bezpośrednio kontaktować się z ośrodkami prowadzącymi rekrutację.
Obecnie mapa jest dostępna jedynie w języku angielskim, ale zgodnie z zapowiedziami, w przyszłych aktualizacjach zostaną dodane kolejne języki UE.
Mapa badań klinicznych w CTIS
Mapa badań klinicznych jest dostępna pod adresem: https://euclinicaltrials.eu/search-for-clinical-trials/trial-map/
Przejrzystość i nadzór nad badaniami klinicznymi
System CTIS działa w ramach Rozporządzenia w sprawie badań klinicznych, udostępniając publiczną bazę danych dostępną zarówno dla specjalistów medycznych, jak i pacjentów. Państwa członkowskie UE i EOG są odpowiedzialne za zatwierdzanie i nadzorowanie badań, natomiast EMA zarządza platformą CTIS i dba o jej rozwój.
Cel inicjatywy ACT EU
Projekt mapy jest częścią planu działań Accelerating Clinical Trials in the European Union (ACT EU) na lata 2025–2026. Jego celem jest poprawa przejrzystości badań klinicznych i ułatwienie dostępu do nowoczesnych terapii dla pacjentów w całej Europie.
Europejska Agencja Leków (EMA) organizuje 7 marca 2025 r. webinar, podczas którego przedstawi szczegółowe informacje o nowej funkcjonalności i jej zastosowaniu w praktyce. Po wydarzeniu nagranie będzie dostępne online.
Źródło:
- https://www.ema.europa.eu/en/news/new-clinical-trial-map-launched-eu